

2025年10月20日,德国柏林——在2025年欧洲肿瘤内科学会(ESMO)年会上,由哈尔滨医科大学附属肿瘤医院张清媛教授领衔的III期BRIGHT-3研究(NCT05257395)公布了预设期中分析结果(490P)。该结果标志着轩竹生物自主研发的新型CDK4/6抑制剂吡洛西利在HR+/HER2-晚期乳腺癌一线治疗中取得重大突破。
ESMO会议 BRIGHT3 poste
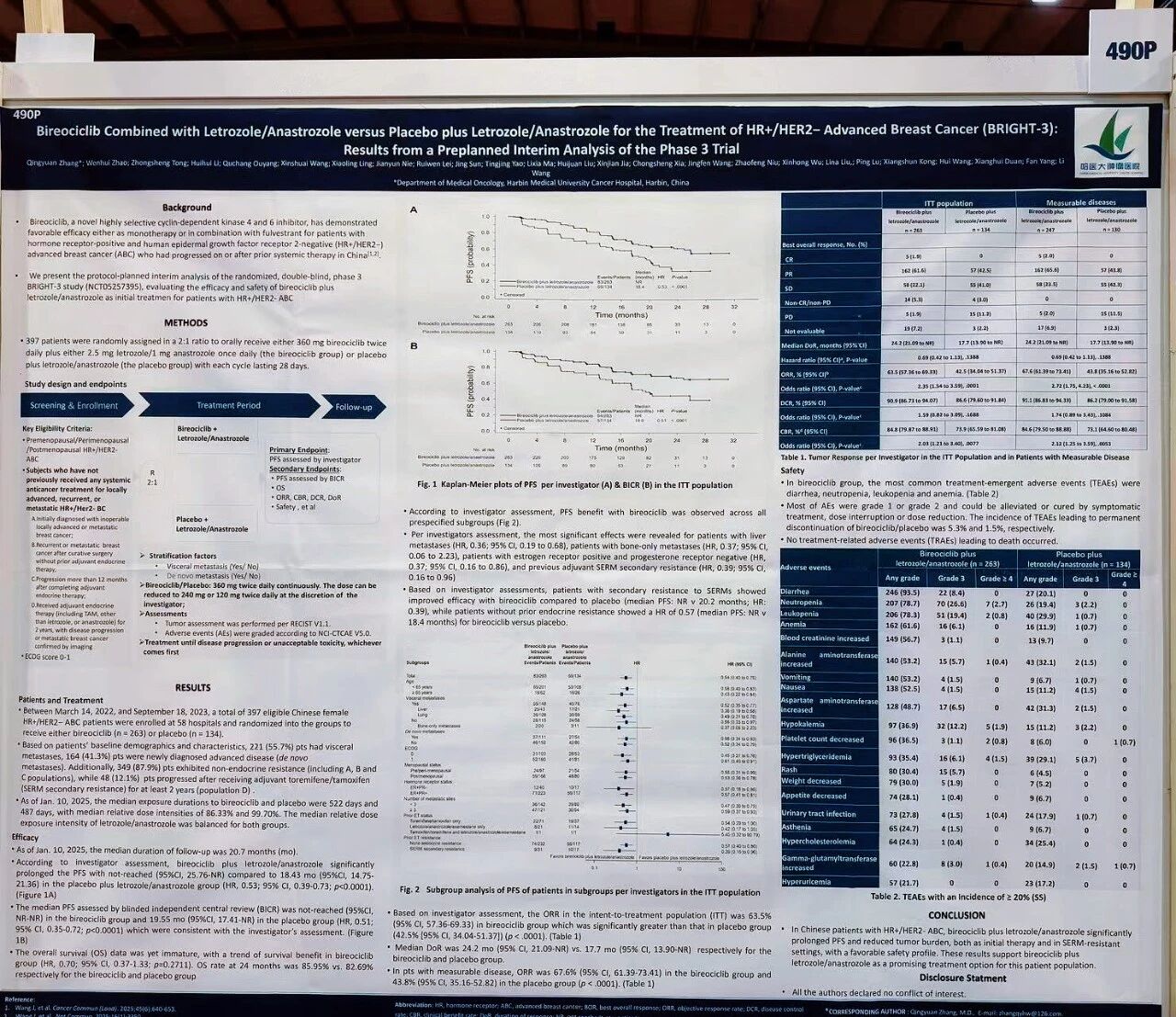
研究证实,吡洛西利联合来曲唑或阿那曲唑,不仅在无进展生存期方面展现出显著优势,还在多个关键亚组中观察到全面获益,同时具备良好的安全性与用药便利性,为中国患者提供了一线治疗的高质量新选择。
主要疗效数据亮眼,无进展生存期显著延长
• 中位无进展生存期:截至2025年1月10日,中位随访20.7个月时,吡洛西利组由研究者和独立评审委员会评估的mPFS均尚未达到,对照组分别为18.43个月和19.55个月。
• 疾病进展风险显著降低:与安慰剂联合内分泌治疗相比,吡洛西利方案可降低47%的疾病进展或死亡风险。
• 客观缓解率大幅提升:在意向治疗人群中,吡洛西利组的ORR达63.5%,显著优于对照组的42.5%。
• 亚组全面获益:在所有预设亚组中均显示出一致PFS获益,尤其在预后较差的肝转移患者中,疾病风险大幅降低64%,显示出其在难治人群中的突出潜力。
安全性良好,便于长期治疗管理
安全性分析显示,吡洛西利联合方案常见不良事件(如腹泻、中性粒细胞减少等)多为1-2级,可通过支持治疗或剂量调整有效管理,整体安全性可控。其口服给药的便利性,也有助于提升患者依从性与生活质量,更契合晚期乳腺癌的慢病化管理理念。
新药审评进展顺利,患者新希望可期
吡洛西利联合芳香化酶抑制剂(AI)治疗HR+/HER2-晚期乳腺癌的新药上市申请已于2025年5月14日获得国家药品监督管理局正式受理。BRIGHT-3研究的卓越数据为其审评提供了坚实依据。期待该药的新适应症能早日获批,为中国HR+/HER2-晚期乳腺癌患者提供疗效卓越、安全便捷的一线治疗新选择,助力提升整体诊疗水平。
关于轩竹生物
轩竹生物是一家根植于中国、具有全球化视野的创新型制药企业,聚焦于消化、肿瘤及非酒精性脂肪性肝炎等重大疾病领域,致力于研发、生产及商业化具有核心自主知识产权的1类新药。公司拥有一流的研发团队,核心人员均具有多年新药研发经验。公司同时具备小分子化药和大分子生物药两大研发体系,双引擎推动公司创新发展,形成了国内少有的同时涵盖小分子化药、大分子生物药、抗体偶联药物(ADC)等多种类型的产品管线。公司以未满足的临床需求为导向,致力于发展成为一家具有自主研发、生产和销售能力的一流创新药企业。

北京朝阳区八里庄西里住邦2000商务中心2号楼21层
9th Floor, North Tower of CP Center, No.20 Jin He East Avenue,Chaoyang District,Beijing,China
电话(T):010-5765 4567
邮箱(E):XZGROUP@xuanzhubio.com
Copyright © 轩竹生物科技有限公司保留所有权利 冀ICP备2020028968号 网站建设技术支持:唯引互动

